studio in corso
studio concluso
Federico Manai, Università di Pavia
Borsa di Studio triennale
Studio sulla Celiachia
Area: Oncologia
Scheda dello Studio
- Numero del Finanziamento (Grant): FC 001/2018
- Titolo: Effetti cellulari e molecolari delle esorfine del glutine sulla tumorigenesi: uno studio pilota in vitro.
- Area Scientifica: Oncologia
- Durata: Progetto Triennale
- Ricercatore Titolare: Dott. Manai Federico, Dipartimento di Biologia e Biotecnologie “L. Spallanzani”, Università di Pavia, Pavia.
- Tutor (Capo Laboratorio): Prof. Sergio Comincini, Dipartimento di Biologia e Biotecnologie “L. Spallanzani”, Università di Pavia, Pavia.
Pubblicazioni:
- Manai F, Zanoletti L, Morra G, Mansoor S, Carriero F, Bozzola E, Muscianisi S, Comincini S. Gluten Exorphins Promote Cell Proliferation through the Activation of Mitogenic and Pro-Survival Pathways. Int J Mol Sci. 2023 Feb 15;24(4):3912. doi: 10.3390/ijms24043912. PMID: 36835317; PMCID: PMC9966116. https://pubmed.ncbi.nlm.nih.gov/36835317/
- Zanoletti L, Valdata A, Nehlsen K, Faris P, Casali C, Cacciatore R, Sbarsi I, Carriero F, Arfini D, van Baarle L, De Simone V, Barbieri G, Raimondi E, May T, Moccia F, Bozzola M, Matteoli G, Comincini S, Manai F. Cytological, molecular, cytogenetic, and physiological characterization of a novel immortalized human enteric glial cell line. Front Cell Neurosci. 2023 Apr 20;17:1170309. doi: 10.3389/fncel.2023.1170309. PMID: 37153631; PMCID: PMC10158601. https://pubmed.ncbi.nlm.nih.gov/37153631/
Lo studio
Cosa si è voluto studiare e perché?
Le esorfine del glutine (GEs) sono piccoli peptidi rilasciati dalla digestione enzimatica del glutine nel tratto gastro-intestinale. È stato dimostrato che questi peptidi sono in grado di entrare nel circolo sanguigno e di legarsi ai recettore per gli opiodi, portando alla loro attivazione. Considerando queste loro proprietà e il fatto che la stimolazione di questi recettori è associata all’attivazione di processi cellulari che promuovono la proliferazione e la percezione del dolore, è stato ipotizzato negli ultimi anni che le GEs possano svolgere un ruolo nell’insorgenza della celiachia asintomatica. I soggetti affetti da questa forma della malattia non sperimentano alcun sintomo nonostante la presenza dei danni caratteristici a livello intestinale. Come è noto, la celiachia non trattata e stati di infiammazione cronica intestinale sono associati a due complicanze della malattia, il linfoma a cellule T associato ad enteropatia (EATL) e il carcinoma dell’intestino tenue (SBC). Un numero sempre maggiore di studi ha dimostrato l’associazione tra i processi cellulari regolati dall’attivazione dei recettori per gli opiodi e il cancro. Considerando queste premesse così come l’assenza nella letteratura scientifica di studi volti a chiarire il ruolo delle GEs nell’insorgenza della celiachia, questo studio ha voluto investigare l’effetto di questi peptidi in modelli cellulari di epitelio intestinale e linfociti T. Inoltre, visto il ruolo sempre più centrale delle cellule enteriche gliali (EGCs) nella corretta fisiologia intestinale, si è studiata anche la loro risposta alle GEs. Le EGCs, infatti, costituiscono insieme ai neuroni enterici, il sistema nervoso enterico e partecipano alla regolazione di numerosi processi fisiologici e patologici. Il loro ruolo in patologie intestinali come il morbo di Crohn e la colite ulcerative è maggiormente noto rispetto a quello nella celiachia, di cui è presente un solo lavoro nella letteratura scientifica.
La Metodologia
Per lo studio sono state selezionate due linee cellulari immortalizzate usate in letteratura come modelli di epitelio intestinale e linfociti T (i.e., Caco-2 e SUP-T1). Per le EGCs è stato creato un modello immortalizzato di queste cellule, chiamato ClK, utilizzando un protocollo di trasformazione validato in letteratura. Le GEs sono state poi saggiate in ognuno di questi modelli cellulari a concentrazioni crescenti. Sono state poi condotte diverse analisi per studiare i processi proliferativi e di morte cellulare.
Quali Risultati e Quali Conclusioni?
Lo studio ha dimostrato che nel modello di linfociti T (i.e., SUP-T1) le GEs non esercitano alcun effetto citotossico anche quando testate ad alte concentrazioni, portando all’attivazione dopo quattro ore di proteine implicate nella proliferazione cellulare e nella resistenza alla morte e ai danni cellulari. Una di queste esorfine, nota come B5, si è rivelata essere la più potente nello svolgere queste attività biologiche, come già noto nella letteratura scientifica. Questa esorfina è stata quindi testata nel modello di epitelio intestinale (i.e., Caco-2), dove si è visto indurre un aumento della vitalità e una diminuzione di proteine implicate nella corretta fisiologia delle cellule dell’epitelio intestinale. Considerando questi risultati è possibile ipotizzare che le GEs giochino un ruolo nell’insorgenza della celiachia, promuovendo l’attivazione dei linfociti T, i maggiori responsabili del danno intestinale, e un’alterazione nella corretta funzionalità delle cellule epiteliali intestinali. Per quanto riguarda le EGCs, l’esorfina B5 è stata testata nella linea cellulare ClK e, a partire da un’ora post-trattamento, è stato osservato un aumento della vitalità cellulare, anche ad alte concentrazioni. Nessuna risposta citotossica è stata registrata. Un’analisi di espressione genica è stata poi effettuata per studiare le risposta delle ClK al trattamento con l’esofina B5. I dati raccolti dopo un’ora dal trattamento suggeriscono una diminuzione dell’espressione di geni coinvolgi nella progressione del ciclo cellulare e un aumento in un gene coinvolto nelle fasi precoci dell’infiammazione intestinale. Questi risultati suggeriscono che l’effetto delle GEs sulle cellule enteriche gliali potrebbe giocare un ruolo importante nell’insorgenza della malattia celiaca.
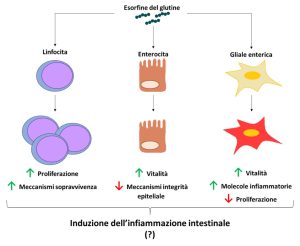
Figura 1. Effetti delle esorfine del glutine nelle tipologie cellulari studiate nel Progetto. I risultati ottenuti dimostrazione che le esorfine promuovano la proliferazione dei linfociti, alterino i meccanismi cellulari che garantiscono l’integrità dell’epitelio intestinale negli enterociti e promuovano una risposta infiammatoria da parte delle cellule enteriche gliali.
Quali prospettive e quali benefici per i pazienti?
Questo studio suggerisce per la prima volta un possibile coinvolgimento delle GEs nell’insorgenza della celiachia, aumentando così le conoscenze riguardo i meccanismi fisio-patologici della malattia. Considerando i risultati ottenuti e la teoria che associa l’attività delle GEs con la celiachia asintomatica, prende maggior corpo l’ipotesi che questi peptidi e i relativi recettori giochino un ruolo nel determinare l’insorgenza di questa forma della malattia. Prospettive future potrebbero riguardare lo studio di mutazioni nei geni codificanti per i recettori per gli opiodi in soggetti affetti da celiachia asintomatica, al fine di determinare un’associazione. Particolari mutazioni, infatti, potrebbero portare a un maggior legame delle GEs con questi recettori, promuovendo la loro attività biologica. L’eventuale dimostrazione di questa ipotesi potrebbe contribuire all’identificazione di un nuovo sistema per stratificare i pazienti celiaci, con possibili ricadute sul piano clinico.
Eventuali sviluppi futuri del progetto
Ulteriori studi legati a questo Progetto potrebbero essere volti a investigare ulteriormente l’effetto delle GEs nei modelli cellulari descritti in precedenza, al fine di indicare nuovi meccanismi cellulari alterati della loro attività biologica. Inoltre, si potrebbe saggiare l’attività biologica delle GEs in modelli sempre più complessi e aderenti alla condizione in vivo (e.g., linee cellulari primarie, organoidi…) al fine di validare quando osservato nei modelli cellulari utilizzati in questo Progetto.
Legenda
Cellula enterica gliale: cellula che, insieme ai neuroni, costituisce il sistema nervoso enterico. Queste cellule partecipano alla regolazione di funzioni intestinali in contesti fisiologici e patologici.
Enterocita: Cellula che costituisce l’epitelio intestinale
Linfocita T: cellula del sistea immunitario implicata nella progressione della malattia celiaca
Organoidi: modelli di microtessuto in 3D derivati a biopsie intestinali
