studio concluso
Lucia Sacchetti, CEINGE-Biotecnologie Avanzate, Napoli
Progetto Biennale
Studio sulla Celiachia
Area: Infiammazione
- Numero del Finanziamento (Grant): FC 007/2014
- Titolo: Studio del microbioma intestinale nella patogenesi della celiachia nell’adulto
- Area Scientifica: Genetica della Celiachia
- Durata: Progetto Biennale
- Ricercatore Titolare: Dott.ssa Lucia Sacchetti, CEINGE-Biotecnologie Avanzate, Napoli
- Collaborazioni: Giovanna Del Vecchio Blanco, Unità di Gastroenterologia, Università di Roma Tor Vergata; Paola Salvatore, Dipartimento di Medicina Molecolare e Biotecnologie mediche, Università di Napoli “Federico II”
Pubblicazioni originate dal Grant:
- V. D’Argenio et al. Metagenomics Reveals Dysbiosis and a potentially pathogenic N. flavescens strain in duodenum of adults celiac patients. The American Journal of Gastroenterology (2016); doi:10.1038/ajg.2016.95 https://pubmed.ncbi.nlm.nih.gov/27045926/
- V. D’Argenio et al. No change in the mucosal gut mycobioma is associated with celiac disease-specific microbiome alteration in adult patients. The American Journal of Gastroenterology (2016); doi:10.1038/ajg.2016.227 https://pubmed.ncbi.nlm.nih.gov/27808136/
- Iaffaldano L, Granata I, Pagliuca C, et al. Oropharyngeal microbiome evaluation highlights Neisseria abundance in active celiac patients. Sci Rep. 2018;8(1):11047. Published 2018 Jul 23. doi:10.1038/s41598-018-29443-1 https://pubmed.ncbi.nlm.nih.gov/30038321/
- Labruna G, Nanayakkara M, Pagliuca C, et al. Celiac disease-associated Neisseria flavescens decreases mitochondrial respiration in CaCo-2 epithelial cells: Impact of Lactobacillus paracasei CBA L74 on bacterial-induced cellular imbalance. Cell Microbiol. 2019;21(8):e13035. doi:10.1111/cmi.13035 https://pubmed.ncbi.nlm.nih.gov/31042331/
Lo studio
Cosa si è voluto studiare e perché?
Il corpo umano rappresenta un ecosistema nel quale coesistono trilioni (1018) di batteri ed altri microrganismi (microbiota) che popolano il nostro organismo. In particolare, il sistema digestivo (tratto gastrointestinale) è formato da diverse nicchie funzionalmente distinte: la cavità orale, lo stomaco, il piccolo intestino ed il colon, ciascuna popolata da microrganismi in parte diversi, che contribuiscono allo svolgimento di numerose importanti funzioni, quali: la sintesi di vitamine, la decomposizione di sostanze chimiche e di nutrienti, il metabolismo dei grassi, lo sviluppo del sistema immune, la lotta a germi patogeni, etc. Il microbiota umano è variabile nelle diverse nicchie e nei diversi individui, essendo modificato da: dieta, antibiotici, stile di vita, etc. Stabilire quindi l’esatta composizione del microbiota in condizioni di salute o in corso di malattie, rappresenta una sfida. Nella celiachia, in aggiunta alla predisposizione genetica (in gran parte legata alla presenza delle molecole di suscettibilità HLA DQ2/DQ8) ed all’ingestione del fattore scatenante “glutine”, ad alcune infezioni virali, anche il microbiota intestinale è stato suggerito svolgere un ruolo importante. Oggi, grazie a tecniche molto sensibili di sequenziamento del DNA batterico (tecniche metagenomiche), è possibile studiare tutto il microbioma intestinale, al contrario delle classiche tecniche microbiologiche (basate sulla coltivazione delle specie batteriche su terreni selettivi), che consentono di studiare solo le specie coltivabili.
Ciò premesso, gli obiettivi del nostro studio sono stati i seguenti: (1)- studiare il microbioma intestinale di soggetti adulti appartenenti a tre gruppi, soggetti celiaci attivi (CD), celiaci a dieta senza glutine (GFD) e soggetti controllo, con tecniche metagenomiche. Ciò al fine di valutare se esisteva un profilo microbico alterato associato alla malattia celiaca. (2) Studiare negli stessi tre gruppi di soggetti (CD, GFD e controlli) la comunità batterica intestinale anche con tecniche classiche di coltura. Ciò al fine di paragonare i dati microbiologici colturali (microbiota) con quelli genetici (microbioma) (di cui al punto1) ed eventualmente isolare ed identificare le specie batteriche differenti tra CD, GFD e controlli. (3) Valutare, nel caso di isolamento di specie batteriche associate alla celiachia, se esse avevano potere infiammatorio e capacità di influenzare talune funzioni dell’epitelio intestinale.
La Metodologia
Lo studio è stato approvato dal Comitato Etico dell’Università Federico II di Napoli e, previa raccolta del consenso informato, sono stati arruolati 97 soggetti (34 CD attivi, 28 GFD e 35 controlli). Il microbioma intestinale è stato valutato, nei campioni duodenali di 41 soggetti e nei tamponi orofaringei di ulteriori 56 soggetti, sia con tecniche metagenomiche (studio del 16S rRNA) che con tecniche colturali. Le sequenze di DNA batterico sono state analizzate tramite programmi bioinformatici (QIIME v.1.9.1). Il potere infiammatorio della specie batterica CD-associata (Neisseria flavescens-Nf) è stato testato su cellule dendritiche di topo ed umane, nonché su espianti intestinali (in vitro). Il traffico intracellulare della Nf isolata dai CD e dai controlli è stato valutato in cellule epiteliali CaCo2 ottenute dalla Banca Cellule del CEINGE, Napoli.
Quali Risultati?
Nei celiaci in fase attiva il phylum più abbondante è risultato il Proteobacteria, seguito da quello dei Bacteroidetes, mentre Actinobacteria e Firmicutes erano quelli meno presenti. Sono stati poi identificati classe, ordine, famiglia e genere in ogni phylum. All’interno della classe dei Beta-proteobacteria, l’ordine Neisseriales, la famiglia Neisseriaceae e il genere Neisseria, sono risultati essere significativamente più presenti nei CD attivi che negli altri due gruppi. Altro risultato interessante è stato quello che nell’orofaringe dei soggetti CD attivi abbiamo trovato un simile profilo microbico, caratterizzato dall’aumento dei Proteobacteria e in particolare del genere Neisseria. L’esame colturale ha consentito di stabilire la vitalità microbica delle Neisserie e di identificare la N.flavescens (Nf) come specie più abbondante nei soggetti CD attivi rispetto agli altri due gruppi. Nella Figura 1 sono riassunti i risultati ottenuti.
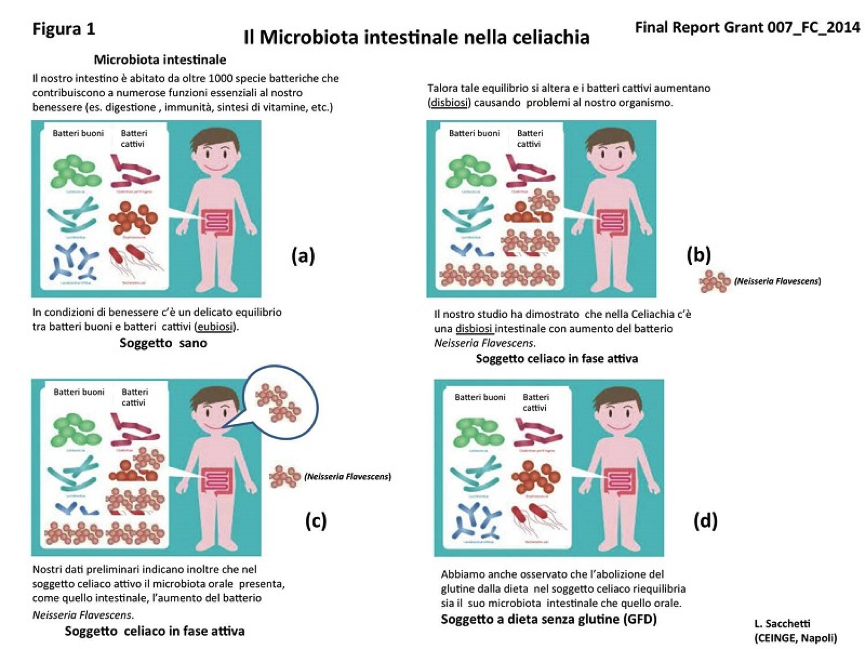 Figura 1 – Composizione del microbioma intestinale (duodenale) in controlli (a), celiaci attivi (b) e a dieta senza glutine (GFD) (d).In (c) il microbiota orale presenta un’alterazione microbica (aumento della Neisseria Flavescens) simile a quella osservata nell’intestino.
Figura 1 – Composizione del microbioma intestinale (duodenale) in controlli (a), celiaci attivi (b) e a dieta senza glutine (GFD) (d).In (c) il microbiota orale presenta un’alterazione microbica (aumento della Neisseria Flavescens) simile a quella osservata nell’intestino.
A questo punto abbiamo voluto approfondire quale potesse essere il significato dell’aumento della Nfnei celiaci attivi, valutandone alcune caratteristiche. Dapprima ne abbiamo esplorato la capacità infiammatoria. Ciò è stato effettuato con due diversi approcci: in primo luogo abbiamo usato cellule dendritiche (DCs)(sia di topo che umane), entrambe sono state trattate per 48 ore con la Nf (lisato) isolata dal duodeno di soggetti celiaci attivi, e poi nel surnatante sono stati misurati i livelli di IL-12p40 e TNF-α (indicatori di infiammazione), che sono risultati significativamente più alti rispetto a quelli misurati in DCs non trattate. In secondo luogo abbiamo esposto espianti di mucosa duodenale ex-vivo di soggetti controllo alla Nf valutando poi l’aumento di marcatori di infiammazione quali l’ HLA-DR e COX-2. Nella Figura 2 sono riassunti i risultati ottenuti. Successivamente abbiamo esplorato l’internalizzazione e la localizzazione intracellulare della Nf osservando che esse sfuggono al compartimento lisosomiale ed anche questo può rappresentare fonte di stress (V. D’Argenio et al.; AJG 2016).
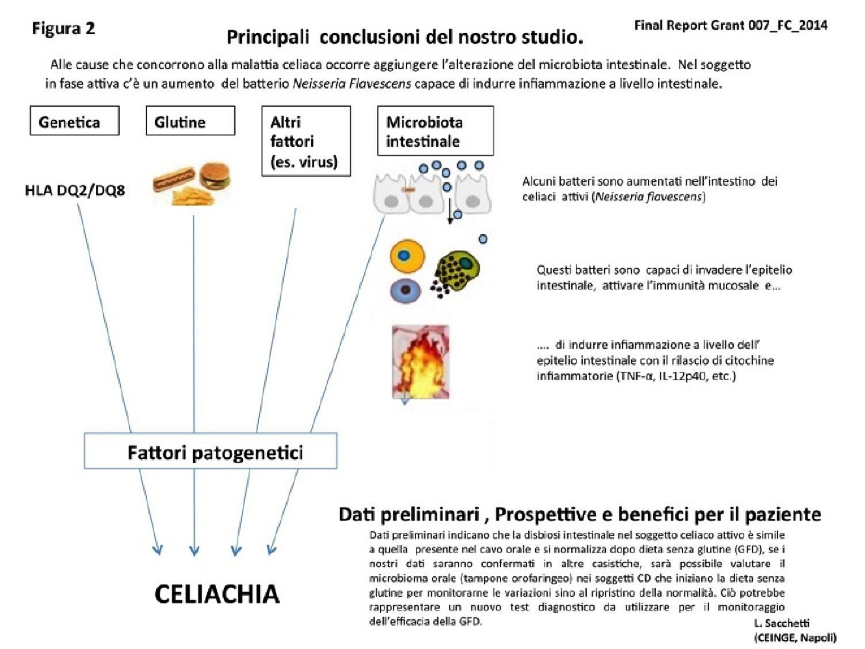
Figura 2 – Il microbiota intestinale e gli altri fattori patogenetici nella celiachia. La Neisseria flavescens (Nf) isolata dai pazienti celiaci attivi induce un profilo pro-infiammatorio in cellule dendritiche (DCs) e nell’epitelio intestinale con il rilascio di marcatori di infiammazione (TNF-α, IL-12p40).
Quali prospettive e quali benefici per i pazienti celiaci?
Il nostro studio ha individuato alterazioni nel microbiota intestinale dei soggetti celiaci che sono caratterizzate in particolare dall’aumento di un batterio: la Neisseria flavescens. Abbiamo dimostrato che tale batterio è capace di indurre infiammazione nell’epitelio intestinale di soggetti sani, indipendentemente quindi da altri fattori predisponenti alla celiachia. Se quest’alterazione batterica precede (causa) o segue (conseguenza) le alterazioni a livello intestinale caratteristiche della patologia non è possibile ancora dirlo, ma certamente essa rappresenta un fattore associato che concorre allo stato infiammatorio dell’epitelio intestinale. Di grande interesse è anche aver stabilito che a livello del tratto gastrointestinale c’è una linea di continuità tra il microbioma del cavo orale (orofaringe) e quello del duodeno, infatti, abbiamo trovato un profilo microbico molto simile in questi due siti. Quest’ultimo risultato può rappresentare un grande vantaggio per il paziente, in quanto raccogliere un tampone faringeo da utilizzare per lo studio del microbioma è certamente una procedura meno invasiva di quella per la raccolta della biopsia duodenale.
Eventuali sviluppi futuri del progetto
Molti dati relativi al microbioma nella celiachia sinora presenti in letteratura sono caratterizzati da scarsa riproducibilità, dovuta a diversi fattori: l’impiego di metodologie diverse, diversi campioni biologici studiati (feci, saliva, duodeno) e differenti gruppi di pazienti arruolati (per età, sesso,criteri di inclusione, etc.), per cui certamente confermare i dati da noi ottenuti su altre coorti di pazienti rappresenta una progettualità importante da sviluppare in futuro. Ma lo sviluppo a nostro avviso più importante sarà quello relativo alle informazioni ottenibili dal microbioma orale che, dai nostri risultati, sembra comparabile a quello ottenuto nel duodeno. In particolare, uno dei nostri obiettivi futuri sarà quello di valutare il microbioma orofaringeo nei soggetti CD che iniziano la dieta senza glutine per monitorarne le variazioni sino al ripristino della normalità. Ciò potrebbe rappresentare un nuovo test diagnostico da utilizzare per il monitoraggio dell’efficacia della GFD.
Legenda
Microbiota Con il termine microbiota umano ci riferiamo alla composizione microbica che prospera sul e nel nostro organismo, in pratica la classificazione tassonomica delle varie specie, per lo più batteriche, ma anche in misura minore archeobatteri, virus e miceti che ci abitano. Si tratta in pratica di trilioni di cellule microbiche. L’aggettivo umano serve a chiarire che si tratta di un microbiota (in particolare quello intestinale) che è abbastanza diverso da quelli riscontrati in diversi habitat naturali e che, probabilmente, è evoluto insieme al genoma umano.
Microbioma Con il termine microbioma ci riferiamo alla caratterizzazione dei microbi a livello genico, cioè alla identificazione del genoma microbico.
Tecniche Metagenomiche Con questo termine ci si riferisce alle tecniche molecolari di indagine del microbiota, all’inizio ci si riferiva al sequenziamento completo di tutto il genoma microbico, poi questo termine è stato esteso anche alla caratterizzazione genetica microbica tramite marcatori genetici quali il 16S rRNA.
Tecnica di sequenziamento della regione 16S rRNA E’ una tecnica metagenomica. Si tratta della caratterizzazione genetica microbica tramite impiego di marcatori genetici quali il gene 16S rRNA (RNA ribosomiale). Questo gene (che ha un basso tasso di mutazione) contiene zone altamente conservate (universali e che quindi non ci consentirebbero di identificare le varie specie batteriche in quanto uguali in tutti i batteri), regioni semiconservate (hanno sequenza uguale tra batteri dello stesso Taxon-Regno) e regioni variabili (che sono uguali solo in batteri della stessa specie. Queste ultime regioni, di qualche centinaia di basi, sono nove V1-V9, e ci consentono di discriminare tra diversi taxa batterici. Con questa tecnica si riesce infatti a definire, nell’ambito del regno dei batteri, i diversi phyla, le classi , gli ordini, le famiglie, i generi e le specie che compongono il microbioma di un distretto corporeo.
Cellule dendritiche (DCs) Cellule che appartengono al sistema immunitario e hanno la funzione di presentare l’antigene ai linfociti B e T. Le cellule dendritiche nascono dalle cellule staminali emopoietiche nel midollo osseo e sono le più importanti dell’insieme delle APC (Antigen presenting cell), insieme ai macrofagi e ai linfociti B. Il loro nome deriva dalla particolare forma ramificata che assumono.
HLA-DR Molecola del sistema maggiore di istocompatibilità di classe II.
COX-2 Enzima indotto rapidamente in monociti o macrofagi da stimoli pro-infiammatori.
